 ARTÍCULO ORIGINAL
ARTÍCULO ORIGINAL ARTÍCULO ORIGINAL
ARTÍCULO ORIGINAL
Factores involucrados en el proceso de reclutamiento de un gipsófito endémico en España: Teucrium libanitis
Factors involved in recruitment process of an endemic gypsophyte species in
Spain:
Teucrium libanitis
Revista Cubana de Ciencias Forestales
Año 2013, Volumen 1, número 1
Pablo Ferrandis Gotor
Dr. en Biología, Sección de Biología de la Conservación de Plantas y Ecología Vegetal, Instituto Botánico de la Universidad de Castilla-La Mancha, Jardín Botánico de Castilla-La Mancha. Campus Universitario, s/n. 02071 Albacete (España). Correo electrónico: pablo.ferrandis@uclm.es
RESUMEN
Los suelos ricos en yesos en ecosistemas áridos y semi-áridos suponen una importante restricción al establecimiento de plantas vasculares. Hasta la fecha, existe poca información sobre cómo operan los factores que controlan el reclutamiento de las especies gipsófitas. El reclutamiento de nuevos individuos, es el resultado combinado de los procesos que participan en la dinámica de bancos de semillas del suelo y en los patrones de establecimiento de las plántulas. En este estudio, se examinaron los patrones espaciales y temporales del reclutamiento de la especie Teucrium libanitis Schreb. (Labiatae), un gipsófito endémico del sureste semi-árido de la Península Ibérica, desde la perspectiva de la dinámica del banco de semillas. Durante todo un ciclo biológico, se monitoreo la producción de semillas, los bancos de semillas, tanto edáfico como aéreo, la predación de semillas y la emergencia de plántulas. En el estudio se consideraron diferentes microhábitats, a fin de determinar los lugares más adecuados para el reclutamiento de T. libanitis. Al final del estudio se llega a la conclusión de que el gipsófito T. libanitis forma un banco aéreo de semillas transitorio y uno edáfico persistente, lo que supone una estrategia bien adaptada a estos ambientes semi-áridos. Por otro lado, la existencia de un banco edáfico de semillas persistente, corrobora la teoría de que el reclutamiento se produce en momentos en las que las condiciones climáticas son especialmente benignas. Las semillas se redistribuyen horizontalmente, acumulándose bajo cubierta vegetal; sin embargo, la supervivencia de las plántulas no viene determinada por los diferentes microhábitats en los que emergen. El reclutamiento no está limitado ni por la predación de hormigas granívoras, ni por la pérdida de viabilidad de las semillas, ni por el ataque de patógenos.
Palabras clave: Estepas yesosas, dinámica del banco de semillas, supervivencia de plántulas, predación de semillas, parches de vegetación.
ABSTRACT
Gypsum soils in arid and semi-arid environments impose an important restriction of vascular plants. Factors controlling the recruitment of gypsophytes species are not completely understood. Recruitment is the combined result of processes involved in soil seed-bank dynamics and seedling establishment patterns. We examined the spatial and temporal patterns in the recruitment of Teucrium libanitis Schreb. (Labiatae), a gypsophyte endemic to the semi-arid south-eastern Iberian Peninsula, from the perspective of soil seed-bank dynamics. Seed production, soil seed bank, aerial seed bank, seed predation and seedling emergence and survival were monitored for one biological cycle. Different microhabitats were considered in the study to determine safe sites for T. libanitis recruitment. The gypsophyte T. libanitis forms a transient aerial seed bank and a persistent soil seed bank in gypsum steppe with a strategy well-adapted to semi-arid environments. The existence of this persistent soil seed bank supports the theory that the recruitment is produced by the occurrence of favourable climatic events. Seeds were redistributed horizontally, accumulating under plant cover, but seedling survival was not dependent on these different microhabitats. Recruitment was not limited by predation or by seed death by aging and pathogen attack.
Key words: Gypsum steppes, seed bank dynamic, seed predation, seedling survival, plant patches.
INTRODUCCIÓN
Sobre los suelos ricos en yesos se desarrolla una vegetación altamente especializada principalmente dominada por caméfitos y anuales; muchos de ellos son especies endémicas amenazadas con escasa distribución (Meyer and García-Moya, 1989). La distribución de su hábitat se reduce a las zonas semiáridas con afloramientos de yesos, uno de los hábitats más amenazados en Europa (European Community, 1992). En los últimos años, un número creciente de autores han centrado sus estudios en el conocimiento de las peculiaridades de estos ecosistemas (Palacio et al., 2007; Quintana-Ascensio et al., 2009; Maestre et al., 2011), centrándose algunos en las etapas más tempranas de las especies gipsófitas (Escudero et al., 1999, 2000), pero hay muy pocos estudios en los que se contemple la perspectiva de la dinámica del banco de semillas (Martínez-Duro et al., 2009).
El reclutamiento de nuevos individuos es el resultado combinado de los procesos que participan en la dinámica de bancos de semillas del suelo y en los patrones de establecimiento de las plántulas. El modelo de la dinámica del banco de semillas del suelo, se basa en la diferencia entre las semillas que persisten en el suelo sin germinar, ya sea por factores endógenos (semillas aletargadas) o exógenos, y aquellas que germinan o mueren como resultado de la predación o de la edad (Schafer and Chilcote, 1969). Baskin y Baskin (1998) incorporaron al modelo de los bancos de semillas la muerte de plántulas tras la emergencia.
Los impactos de la granivoría son importantes en los bancos de semillas en hábitats de zonas áridas y semi-áridas. Hormigas, aves y roedores pueden llegar a causar hasta el 95% de las pérdidas de semillas en estos ecosistemas, tanto por predación pre-dispersiva como post-dispersiva (Kemp, 1989). A este hecho hay que sumarle el efecto de los patógenos (hongos), que llegan a destruir una porción del banco de semillas bastante importante (35%) en este tipo de ecosistemas (Crist and Friese, 1993).
Los bancos de semillas aéreos son una manera alternativa de reservar las semillas y se deben a que las semillas no maduran todas al mismo tiempo, sino de manera progresiva, y se mantienen en la planta madre durante un periodo de tiempo más o menos largo (Hamilton et al., 2009).
En las estepas de yesos de las zonas semi-áridas, el éxito del reclutamiento de nuevos individuos viene marcado por el momento y el lugar de la germinación de las semillas. Si ésta se produce de manera temprana, las posibilidades de sobrevivir a la sequía del primer verano, período más crítico para las plántulas, son mayores (Escudero et al., 1999, 2000, 2005). Los parches de vegetación en estos ecosistemas ejercen un papel importante a la hora de determinar la estructura espacial de los bancos edáficos de semillas, ya que actúan como centros de acumulación (Caballero et al., 2008). Sin embargo, en los microhábitats que se producen debajo de estos parches de vegetación, las interacciones entre plantas son complejas, existiendo un efecto positivo de facilitación y uno negativo de competencia (Escudero et al. 2005).
Desde la perspectiva temporal, el establecimiento de nuevos individuos no solo requiere de la presencia de propágulos, sino de la concurrencia de eventos climáticos favorables, tales como lluvias más abundantes durante ciertos momentos del año o temperaturas inusualmente benignas (Goldberg and Turner, 1986). De esta manera, las poblaciones en ecosistemas áridos suelen estar compuestos por cohortes establecidas en años puntuales, con amplios espacios temporales entre momentos favorables (Escudero et al., 1999, 2000; Eugenio et al., 2012).
En este artículo, se estudian los patrones temporales y espaciales del reclutamiento del Teucrium libanitis, un gipsófito endémico ampliamente distribuido por las zonas de yesos del sureste de la Península Ibérica. Concretamente, se trata de determinar los factores que determinan la germinación de las semillas de esta especie, así como aquellos que ocasionan la pérdida de semillas considerando el modelo de Schafer and Chilcote (1969), a fin de ampliar el escaso conocimiento sobre la fase más temprana del reclutamiento de nuevos individuos en estos ecosistemas tan peculiares. Por los resultados previos de otros estudios (Martinez-Duro et al, 2009), se prevé que los microhábitats afectarán a la distribución de las semillas y la emergencia de plántulas. También cabe esperar un efecto positivo de facilitación de los individuos adultos en las semillas y en la posterior emergencia de plántulas.
MATERIAL Y MÉTODO
Especie estudiada
Teucrium libanitis Schreb. (Labiatae) es un caméfito de unos 20-25 cm de altura. Vive sobre suelos ricos en yesos (gipsófito) del sureste español. Es la especie endémica principal de la asociación vegetal ThymoTeucrion verticillati (Rivas-Martínez y Costa, 1970), una comunidad vegetal restringida a los afloramientos de yesos situados en el sureste español.
T. libanitis se reproduce exclusivamente por semillas. Florece y fructifica desde agosto hasta octubre. Los cálices, persistentes, retienen las semillas (2-4), formando un banco aéreo de semillas, y se desprenden por barocoría paulatinamente en el tiempo (Rivas-Martínez, 1974).
Zona de estudio
Este estudio se ha llevado a cabo dentro de la microrreserva de El Yesar de Casicas Nuevas, en el sureste de Albacete (España; coordenadas U.T.M.: 30SXH2061). En esta zona se encuentra un ejemplo bien conservado de una estepa yesosa del semi-árido español; un hábitat protegido tanto a nivel regional (JCMM, 1999) como europeo (European Community, 1992). La superficie total de esta microrreserva es de unas 3 ha valladas para evitar la entrada de ganado. Se distinguen dos zonas en esta área: una colina con una zona superior llana y con una costra de yesos dura, y una zona baja en la que las sales se acumulan por lixiviación. La zona alta, de unos 5,000 m2, está ocupada por un tomillar gipsófilo, dominado por arbustos tales como T. libanitis, Thymus funkii subsp. funkii, Herniaria fruticosa, Helianthemum syriacum, H. squamatum, Onobrychis stenorhiza y Fumana hispidula, agrupadas formando parches de vegetación (cobertura vegetal del 15%) (Ferrandis et al., 2005).
Durante el estudio, dos data-loggers registraron las condiciones ambientales de la zona: temperatura ambiental y del suelo a dos profundidades (modelo Tinytag Plus TGP-0020, rango: 40ºC, +125ºC; Gemini Data Loggers, UK) y lluvia (modelo 400 WatchDog Data Loggers, 1/100 inch increments, Spectrum Technologies Inc, IL, USA).
Producción y lluvia de semillas
Durante el periodo de dispersión del año 2006, se estimaron la producción y la lluvia de semillas (área del suelo donde las semillas caen desde la planta madre) de 5 individuos maduros de T. libanitis en el hábitat natural. Al comienzo de la fase de floración, se cubrió el suelo debajo de cada uno de los individuos seleccionados con una lámina de acetato plástico translúcido (70 cm x 70 cm) impregnado de una sustancia pegajosa (Tanglefoot Company, Michigan, USA). Las láminas se cambiaron periódicamente hasta que la dispersión finalizó y se llevaron al laboratorio, donde las semillas eran contadas y se anotaba la distancia al centro de la planta así como su orientación, usando una cuadrícula de 5 cm x 5 cm.
Banco edáfico de semillas
Se evaluó el banco de semillas del suelo del T. libanitis bajo 20 individuos maduros. Se recolectaron muestras de suelo a dos profundidades (0-4 y 4-8 cm), de manera periódica tras la dispersión de las semillas (enero, mayo y julio de 2006). En cada muestreo, se tomaron cuatro sondas (3 cm de diámetro) a cada una de las profundidades y debajo de cada individuo. Se llevó al laboratorio cada muestra en una bolsa de plástico y se tamizaron con tamices de 0.25 mm de luz. Bajo una lupa binocular, se fueron separando las semillas las que fueron sometidas a un ensayo de germinación para comprobar su viabilidad.
Destino de las semillas en el suelo
Se llevó a cabo un ensayo de enterramiento de semillas durante 24 meses. Se prepararon lotes de semillas consistentes en 1,000 semillas recién recogidas dentro de saquitos de nailon con tierra natural esterilizada y enterradas en el hábitat natural y en un umbráculo bajo condiciones controladas de humedad a dos profundidades distintas (2 y 8 cm) en octubre de 2005. Al final del período de dispersión y al cambiar de estación, un lote de semillas de cada lugar y a cada profundidad era desenterrado. La viabilidad de las semillas rescatadas que no habían germinado era evaluada mediante un ensayo de germinación. De este modo, se pudieron clasificar las semillas en germinadas (testas vacías), germinables (semillas que germinaban en los tests de germinación), latentes (semillas que no germinaban salvo con riego con una disolución de ácido giberélico; GA3 al 1%) y muertas (aquellas que se deshacían cuando se presionaban ligeramente con las pinzas).
Banco de semillas aéreo
Se eligieron diez plantas maduras para seguir la dispersión de los cálices a los largo del tiempo (agosto 2007). Cada mes, se contó el número de cálices remanente en cada planta y después se tomaron 10 cálices para estimar la viabilidad de las semillas remanentes en el banco aéreo.
Predación pre- y post-dispersiva
Observaciones preliminares durante el año 2006, permitieron identificar un único predador de las semillas de T. libanitis, la hormiga granívora Messor bouvieri. La predación pre-dispersiva de cálices con semillas en T. Libanitis no deja señal alguna, por lo que su estima se basó en conteos directos sobre las propias plantas. Cada 3-4 días durante el período de dispersión de los cálices y de actividad de la hormiga (octubre y noviembre de 2007), se anotó el número de plantas que eran visitadas por las hormigas, así como los cálices que se llevaban. También se evaluó el éxito en el transporte de los cálices hasta el nido, mediante el seguimiento de obreras de M. bouvieri (n=40) desde el momento en que recolectaban un cáliz de la planta hasta que llegaban al hormiguero.
Por otro lado, se evaluó la predación post-dispersiva de M. bouvieri colocando 45 trampas en las que había 40 cálices maduros de T. libanitis. Las trampas consistían en placas Petri de plástico de 9 cm de diámetro cubiertas por una malla de 1 mm de luz con un agujero lateral de 1 cm orientado hacia el hormiguero. Las trampas fueron colocadas alrededor del nido en 3 microhábitats diferentes: bajo plantas aisladas de T. libanitis, bajo parches de vegetación con T. libanitis y en suelo desnudo. También se anotó la distancia de cada trampa al hormiguero. Se revisaron las trampas y se contaron los cálices restantes cada 3-4 días durante el periodo de dispersión (octubre-diciembre 2007).
Emergencia y supervivencia de plántulas
Se hizo el seguimiento de la emergencia y la supervivencia de plántulas en 20 parcelas permanentes seleccionados tres microhábitats diferentes: bajo y alrededor (hasta una distancia igual a la mitad de la altura de la planta) de plantas aisladas de T. libanitis, bajo y alrededor de parches de vegetación que incluían individuos de T. libanitis y en cuadrados de 50 cm x 50 cm de suelo desnudo. El control en las 60 parcelas comenzó al finalizar el período de dispersión (noviembre 2007) y finalizó tras superar el período crítico del primer verano, un año después (diciembre 2008).
Se marcaron las plántulas emergentes con pequeñas banderas rojas tan pronto como eran detectadas. Las visitas se efectuaban cada 2-3 días durante el periodo de emergencia, para evitar errores debido a muertes tempranas de las plántulas. Al finalizar el flujo de emergencias, se revisitaron las parcelas con menos frecuencia (primero cada semana, luego cada dos).
Análisis estadístico
Se emplearon modelos lineales generalizados (GLMs) para establecer la relación entre la producción de semillas y el tamaño de la planta. Las variables de las plantas evaluadas fueron: cobertura, calculada en base a los dos ejes elipsoidales; altura y diámetro del cuello de la raíz. Se empleó una transformación logarítmica (log10 [n +1]) con la producción de semillas.
En el caso de los bancos de semillas, se analizó el efecto de la profundidad y la fecha sobre la densidad de semillas mediante un análisis ANOVA de dos vías. Si existían diferencias significativas en la variable fecha, se realizaba un análisis de comparación múltiple (Tuckey). También se comprobaron la normalidad (Cochran test) y la homocedasticidad (David test) de las variables empleadas.
Para explorar los cambios temporales del banco aéreo de semillas en relación con la cobertura vegetal se empleó una regresión simple.
También se utilizó una regresión simple para analizar la dependencia de la emergencia de plántulas en el campo, previamente transformada mediante un logaritmo, con la cobertura vegetal de los parches. El efecto del microhábitat sobre el número de plántulas emergidas fue estudiado mediante una ANOVA de una vía. Las diferencias significativas entre micro hábitats se establecieron mediante un test de comparación múltiple (Tukey test).
En el caso de la supervivencia de las plántulas, se analizó el efecto de los microhábitats y el tiempo en el porcentaje final de supervivientes mediante un análisis de regresión múltiple. Antes de los análisis, se transformó el porcentaje final de plántulas mediante una raíz cuadrada del arcoseno y se comprobó la normalidad (Cochran test) y la homocedasticidad (David test) de las variables empleadas.
Se empleó el programa estadístico STATGRAPHICS plus 5.1 para llevar a cabo todos estos análisis.
RESULTADOS
Producción y lluvia de semillas
La producción media de semillas viables fue de 1029 por planta (SE=196; n=5). Esta producción está positivamente correlacionada con el diámetro del cuello de raíz de las plantas: log10 [seed-prod +1] = 2.637 + 0.112*diam (R2 = 0.8084; p = 0.0242). Las semillas se dispersan por gravedad dentro de los cálices y quedan atrapadas bajo la planta madre, ya que la lluvia de semillas disminuye rápidamente más allá de los 10 primeros cm desde el centro de la planta.
Banco edáfico de semillas
Los resultados del banco edáfico de semillas muestran un banco viable a lo largo del año y a ambas profundidades. Las densidades varían significativamente tanto por la profundidad como a lo largo del tiempo (Figura 1). La viabilidad de las semillas en el banco fue constante (64.05%; SE = 5.50) e independiente de la profundidad (F1, 13 = 0.14; p = 0.710) y del tiempo (F2, 13 = 1.77; p = 0.209), pero significativamente menor que la de las semillas recién maduradas (97.83%; SE = 2.17).
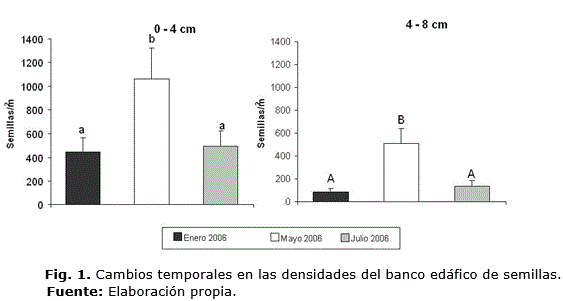
Los valores corresponden a la media de las semillas (n= 30) encontradas en las muestras de suelo tomadas de las capas superiores (0-4 cm) e inferiores (4-8 cm) del suelo. Diferencias en las letras sobre las barras denotan diferencias significativas detectadas en el test de Tukey asociado al ANOVA bifactorial: diferentes letras: diferencia entre fechas; mayúsculas o minúsculas: diferencia entre profundidades.
Destino de las semillas en el suelo
Los ensayos de desenterramiento de las semillas revelan dos patrones diferentes de comportamiento dependiendo de si la humedad es o no un factor limitante. Así en los lotes enterrados en el umbráculo bajo condiciones controladas de riego (sustrato constantemente humedecido), los porcentajes de germinación fueron muy altos tras el primer otoño (80-85%) independientemente de la profundidad de enterramiento, alcanzando casi el 100% tras el segundo otoño. Sin embargo, en el caso de las semillas enterradas en el hábitat natural, lo que se observa es que la germinación va poco a poco aumentando durante el primer año hasta alcanzar el 50% de germinación, alcanzando el 100% de la germinación tras el segundo año, al final del ensayo, independientemente también de la profundidad a la que se encontraran enterradas.
Las fracciones de semillas inviables o muertas suponen un porcentaje muy bajo, en torno al 5%, constante a lo largo de todo el ensayo.
Banco de semillas aéreo
La dispersión de los cálices remanentes en el banco aéreo de semillas ocurre entre septiembre y junio. Esta dispersión de semillas sigue un modelo exponencial: semillas/planta = exp (426.456 0.605*Mes) (F1, 9 = 159.81; P < 0.0001; R2 = 94.1). No encontramos diferencias significativas en la viabilidad de las semillas frescas y las que permanecen en las plantas.
Predación pre- y post-dispersiva
Las hormigas de M. bouvieri predan pocos cálices en la planta. De hecho, tan sólo observamos hormigas sobre tres plantas de T. libanitis. No se produjo ninguna pérdida en el trayecto hasta el hormiguero.
En cuanto a la predación post-dispersiva, las hormigas recogieron el 2.5% (SE=1.5) de los cálices puestos en las trampas. La actividad predadora se concentró en tres trampas y era independiente del tipo de microhábitat (F2, 42 = 0.02; p = 0.99) y de la distancia al hormiguero (F1, 43 = 0.21; p = 0.65).
Emergencia y supervivencia de plántulas
La emergencia de plántulas se produce desde finales de febrero hasta finales de junio, con un pico en mayo y principios de junio (> 80%). El número de plántulas fue mayor en las zonas de los parches de vegetación y casi nula en las zonas de suelo desnudo. El número de plántulas emergentes no depende de la cobertura de T. Libanitis en las parcelas (F1, 38 = 0.21; P > 0.05) pero sí que está positivamente correlacionada con la cobertura vegetal total, independientemente de la especie de la que se trate (Figura 2).
Teucrium = plantas aisladas de T. libanitis, Parches = parches de vegetación, Suelo = suelo desnudo. La figura muestra el modelo de regresión significativo que relaciona el número de plántulas logarítmicamente transformado y la cobertura vegetal total de cada plot (F1, 58 = 82.6; P < 0.001; R2 = 58.0).
Se registra una mortalidad alta de plántulas en todos los microhábitats, lo que reduce la población de plántulas desde mediados de abril en adelante. La mayor mortalidad (80-85% de las plántulas) se registra entre mayo y julio. Las curvas de supervivencia ajustadas para cada microhábitat no muestran diferencias significativas entre las tres líneas de regresión, por lo que podemos establecer un único modelo de curva de supervivencia: arcosen (plántulas-2) = 139.124 0.197*Mes (F1, 28 = 120.3; P < 0.001; R2 = 80.4).
DISCUSIÓN Y CONCLUSIONES
A pesar de que las especies perennes suelen estar poco presentes en los bancos de semillas de las zonas áridas y semi-áridas, los datos obtenidos revelan que T. libanitis forman un banco edáfico de semillas persistente (sensu Thompson et al., 1997). Normalmente la estrategia que presentan estas especies perennes es tener una longevidad muy larga, en la que basan su resilencia (Kemp, 1989; Facelli et al., 2005), aunque también hay especies perennes que forman banco se semillas persistente (Aragón et al., 2007).
Los resultados obtenidos en los ensayos de enterramiento de semillas revelan que las pérdidas de semillas por pérdida de viabilidad o por la acción de los patógenos es bastante baja (5%), lo que contrasta con los resultados obtenidos por Crist y Freise (1993), que estimaban las pérdidas en los bancos de semillas por estos factores en un 35% en el caso de una zona arbustiva del semi-árido. Así mismo, estos ensayos también ponen de manifiesto otro dato interesante y es que el estado de las semillas de T. libanitis no varía ni con el paso del tiempo ni con la profundidad del enterramiento. Solo se encuentran diferencias cuando las condiciones de humedad varían, de manera que si el agua no es un factor limitante, las semillas apenas persisten unos pocos meses en el suelo, mientras que cuando no hay agua pueden persistir hasta 2 años viables. Este hecho revela que T. libanitis es capaz de formar un banco edáfico de semillas bajo condiciones de estrés hídrico. También se han encontrado evidencias que muestran que esta especie puede formar un banco aéreo de semillas transitorio. Ambos hechos, confirman los resultados obtenidos en otros ecosistemas áridos y semi-áridos en los que los periodos de sequía prolongados limitan el establecimiento de nuevos individuos a épocas excepcionalmente benignas (Eugenio et al., 2012).
Las semillas de T. libanitis presentan los patrones de germinación típicos de las especies adaptadas a ambientes semi-áridos mediterráneos (Escudero et al., 1997; Albert et al., 2002). Los estudios en campo muestran el pico germinativo en mayo, lo que podría suponer una desventaja en los ambientes mediterráneos caracterizados por una fuerte sequía estival, ya que una emergencia temprana antes del verano daría a las plántulas muchas más posibilidades de sobrevivir a éste período crítico (Escudero et al., 2005).
La distribución de las plántulas depende de la cobertura vegetal, independientemente de las especies que formen parte del parche de vegetación. Las plantas actúan reteniendo los cálices de Teucrium cuando se mueven horizontalmente, fenómeno que se ha constatado en otras estepas de ambientes semi-áridos (Caballero et al., 2008; Martínez-Duro et al., 2009). La dispersión secundaria por viento o escorrentía es una característica típica de zonas áridas y semi-áridas cuya vegetación es bastante escasa y está agrupada en parches (Aguiar y Sala, 1997).
Aunque la supervivencia de las plántulas no varía entre microhábitats, sí que se ha constatado que depende del momento del año, siendo más baja durante los meses de sequía estival (junio-agosto). Esta observación corrobora el hecho de que el agua es el principal recurso limitante para las plántulas en las regiones áridas, presentando una alta mortalidad debida al estrés hídrico (Chabot y Mooney, 1985). Otras especies gipsófitas muestran también supervivencias muy bajas en estas condiciones, tales como Thymus funkii subsp. funkii (Martinez-Duro et al., 2009), Lepidium subulatum (Escudero et al., 2000) y Helianthemum squamatum (Escudero et al., 1999).
El único predador de las semillas de T. libanitis detectado es la hormiga granívora M. bouvieri. A nivel poblacional, las pérdidas de semillas causadas por la predación son despreciables. Estos resultados contrastan con el patrón general descrito en la literatura, el cual pone en relieve el papel fundamental que juegan los granívoros en los ambientes áridos y semi-áridos (p.ej. Kemp, 1989; López et al., 2000).
En conclusión, este estudio muestra que el gipsófito T. libanitis forma un banco aéreo de semillas transitorio y un banco edáfico de semillas persistente en las estepas yesosas, lo cual supone una buena adaptación a estos ecosistemas. La existencia de estos bancos de semillas corrobora la teoría de que el reclutamiento de nuevos individuos se produce en momentos puntuales bajo condiciones más favorables. Las semillas se redistribuyen horizontalmente, acumulándose bajo la cubierta vegetal, que conforman zonas con mejores condiciones para el reclutamiento en hábitats con escasez de agua; aunque posteriormente su supervivencia no depende del lugar donde germinen. Para esta especie, ni la predación, ni la pérdida de viabilidad de las semillas, ni el ataque de los patógenos supone una limitación para el reclutamiento de nuevos individuos.
REFERENCIAS BIBLIOGRÁFICAS
Recibido: 21 de junio 2013.
Aceptado: 21 de julio2013.
Dr. en Biología, Sección de Biología de la Conservación de Plantas y Ecología Vegetal, Instituto Botánico de la Universidad de Castilla-La Mancha, Jardín Botánico de Castilla-La Mancha. Campus Universitario, s/n. 02071 Albacete (España). Correo electrónico: pablo.ferrandis@uclm.es